 |
| サイトマップ | |
|
 |
| サイトマップ | |
|
代謝経路、潜在的な代謝部位を迅速に特定し、化合物設計をガイドして、代謝障害を回避します。Phase I および Phase II 酵素ファミリー反応の基本的なメカニズムの理解に基づく正確で転用可能な予測により、結果に自信を持つことができます。
さまざまな Phase I および Phase II 酵素ファミリーによる代謝に対して脆弱な部位を特定することにより、安定性の向上に向けた化合物設計を導きます。
実験の優先順位付けのための情報を提供し、薬物間相互作用のリスクを低減します。
|
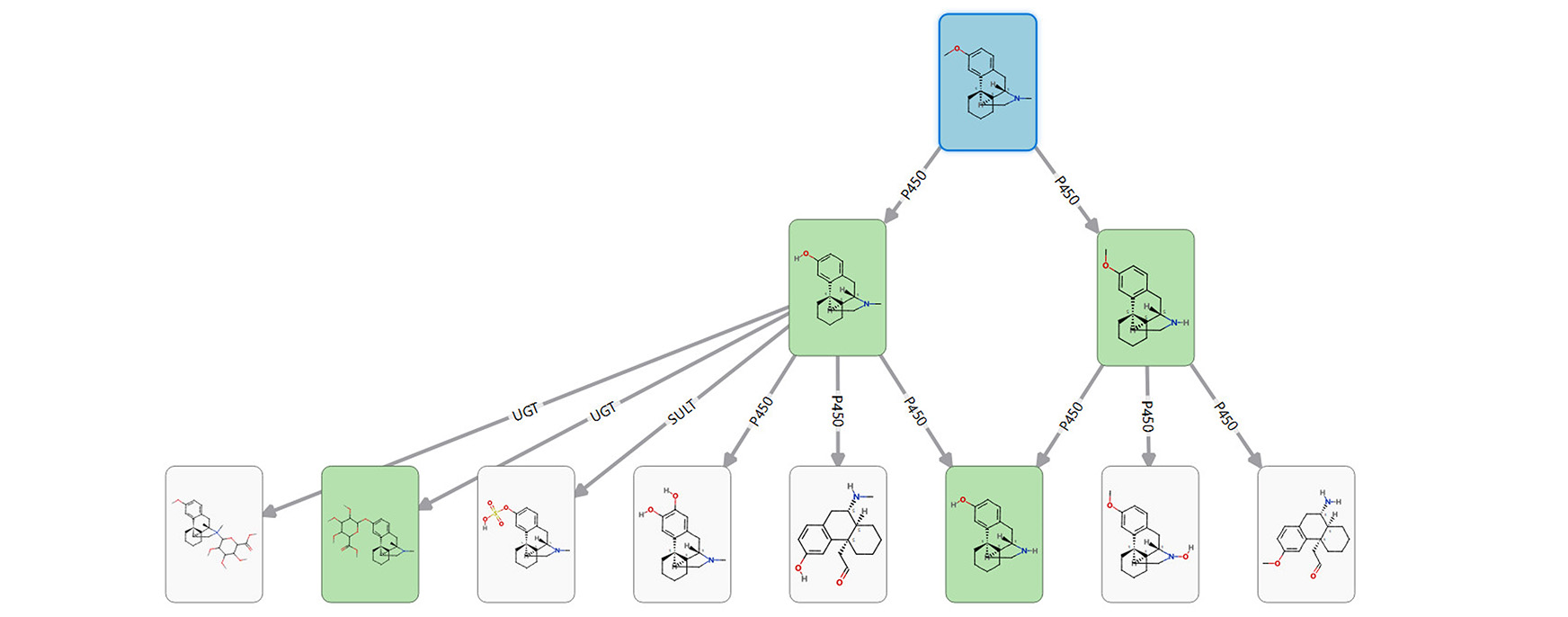
Card View® を使用し、明確で直感的な方法で経路をマッピングできます。
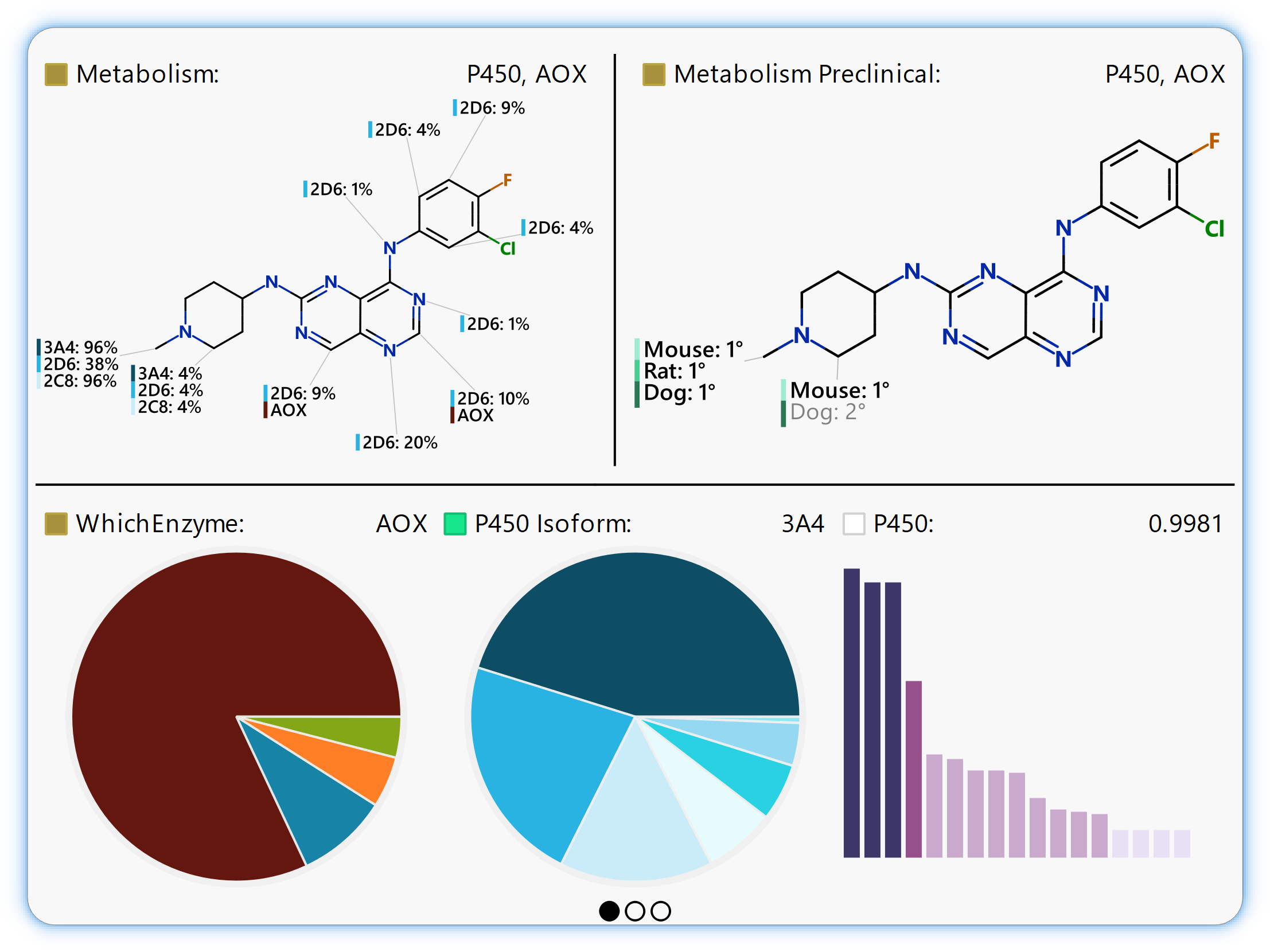
ラット、マウス、イヌのシトクロム P450 モデルを用いた試験に最適な前臨床種を特定します。
WhichEnzyme™ モデルを使用して、薬物代謝に関与する 5 つの主要な酵素ファミリーのうち、ヒトにおける化合物の代謝に関与している可能性が最も高いものを特定します。
WhichP450™ モデルでは、さらにアイソフォーム特異的なレベルに引き上げ、ヒトシトクロム P450 の 7 つの主要な薬物代謝アイソフォームのうち、どれが化合物を代謝する可能性が最も高いかを特定します。
潜在的な薬物間相互作用を回避するために複数の代謝経路を持つ化合物を発見し、実験的試験中にカバレッジを確保するために最も重要な酵素を特定します。
位置選択性モデルを用いて、ヒト CYP、AOX、FMO、UGT、SULT、ラット、マウス、イヌの CYP など、さまざまな酵素ファミリーについて、代謝が起こりやすい部位と対応する潜在的な代謝物を特定します。
代謝経路を高い精度で予測し、実験で観察される可能性が最も高い代謝物を特定するのに役立ちます。これらのモデルの結果は、代謝物同定実験の解釈に役立てることができます。予測を StarDrop の Derek Nexus モジュールと組み合わせて、患者に有害な副作用をもたらす可能性のある代謝物内の毒性エンドポイントを特定します。
位置選択性モデルを使用して代謝の可能性のある部位を特定し、さらなる最適化のための部位に優先順位を付けます。化合物の再設計をガイドし、潜在的に不安定な部位をブロックしながら、StarDrop のコアである確率的スコアリング機能を使用して、重要な化合物特性間のバランスを確保し、マルチパラメーターを最適化します。
薬物間相互作用 (DDI) は、通常、同時投与された薬物が主に同じアイソフォームによって代謝される場合に発生します。薬物は互いのクリアランスを妨げ、薬物濃度の上昇と潜在的な毒性につながる可能性があります。したがって、潜在的な DDI を最小限に抑えるために、化合物は通常、複数の酵素ファミリーまたはアイソフォームによって代謝される必要があります。代謝モジュールの WhichEnzyme および WhichP450 モデルを使用して、複数のクリアランス経路を持つ化合物を同定します。
ラット、マウス、イヌのシトクロム P450 のモデルにより、ヒトの代謝物予測と比較することができ、前臨床試験で代謝物に最も一致する可能性のある前臨床種を特定するのに役立ちます。
基礎的機構の理解に基づいて、StarDrop のモデルは従来の QSAR 法よりも高い精度と転用可能性を持っています。位置選択性モデルにより、ヒトの Phase I および Phase II 相代謝に関与するいくつかの重要な酵素の代謝部位を同定することができます。
さらに、このモジュールにはラット、イヌ、マウスの CYP モデルが含まれているため、一般的な前臨床種の代謝部位を特定し、ヒトの予測と比較することができます。
これらの位置選択性モデルに加えて、StarDrop の WhichEnzyme™ および WhichP450™ モデルは、化合物を代謝する可能性が全体的に最も高い酵素ファミリーまたは特異的なヒト CYP アイソフォームを予測するのに役立ちます。
多世代の代謝経路を生成し、代謝物と親化合物の関係を Card View で簡単に視覚化します。代謝物の過剰予測を避けるために感度と精度を厳密にテストし、結果として得られる潜在的な代謝物に優先順位を付けて、実際に in vivo で観察される可能性が最も高いものを示します。これにより、体内の薬物代謝をよりリアルに表現することができ、ユーザーは最も関連性の高い酵素に対する安定性のために分子を最適化することができます。Derek Nexus モジュールと組み合わせて使用することで、潜在的な代謝物の毒性に関する情報を得ることも可能です。
|